العنصر الكيميائي (Chemical element) هو أي مادة لا يمكن أن يتم تحليلها إلى مواد أبسط عن طريق العمليات الكيميائية العادية، وتعتبر العناصر المواد الأساسية التي تتكون منها كل المادة،[١] ويمكن أن تتكون عناصر كيميائية جديدة بواسطة التفاعلات النووية، ويتم تحديد العناصر من خلال عدد البروتونات التي يتملكها العنصر، حيث تحتوي جميع ذرات عنصر ما على العدد نفسه من البروتونات، لكن يمكن أن تحتوي على أعداد مختلفة من الإلكترونات والنيوترونات.، ويؤدي تغيير نسبة الإلكترونات إلى البروتونات إلى إنشاء الأيونات، في حين أن تغيير عدد النيوترونات يشكل نظائر، ويوجد 115 عنصر معروف، وتجري البحوث الآن لزيادة عدد العناصر إلى 120.[٢]
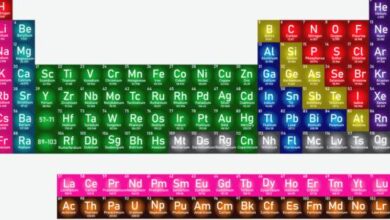
يتم تصنيف العناصر الغذائية في الجدول الدوري، حيث تُسمى العناصر الموجودة في نفس العمود على الجدول الدوري ب”مجموعة”، والتي تمتلك تكوينات إلكترونية متماثلة، فيكونو بالتالي تتصرف بطريقة مشابهة كيميائياً، فمثلاً تعتبر جميع عناصر المجموعة الـ 18 خاملة أو غازات نبيلة، وتُصنف العناصر إلى مجموعات، وهي:[٣]
- المعادن القلوية: تُشكل المعادن القلوية المجموعة الأولى من الجدول الدوري، وتشمل العناصر من الليثيوم (Li) حتى الفرنك (Fr)، وتمتلك هذه العناصر سلوك وخصائص متشابهة جداً، ويوجد الهيدروجين ضمن المجموعة الأولى، لكنه يمتلك خصائص معدنية قليلة، وغالباً ما يُصنف مع اللافلزات.
- المعادن الأرضية القلوية: تشكل المجموعة الثانية من الجدول الدوري، بدءاً من البريليوم (Be) حتى الراديوم (Ra)، وتمتلك الفلزات الأرضية القلوية على نقاط انصهار، وأكاسيد عالية جداً تحتوي على حلول قلوية أساسية.
- اللانثانيدات: يتكون اللانثانيد من العناصر ذات الرقم الذري من 57 وهو اللنثانوم (La),، إلى 71 وهو اللوتيتيوم (Lu)، وغالباً ما يطلق عليهم الأكتينيدات، و”the f-elements”، لأن لديهم إلكترونات تكافؤ في القشرة f.
- الأكتينيدات: تتكون الأكتينيدات من العناصر بعدد الذرات من 89، وهو الأكتينيوم (Ac)، إلى 103 وهو اللورنسيوم (Lr)، وتعتبر جميعها عناصر مشعة.
- الفلزات الانتقالية: العناصر الانتقالية عبارة عن معادن لها مستوى طاقة فرعى مليء جزئياً، وتضم مجموعات من 3 إلى 12، واللانثانيدات، والأكتينيدات.
- الفلزات بعد الانتقالية: تضم هذه العناصر الألومنيوم (Al)، والغاليوم (Ga)، والإنديوم (In)، والثاليوم (Tl)، والقصدير (Sn)، والرصاص (Pb)، والبزموت (Bi)، وتمتلك هذه العناصر بعض خصائص المعادن الانتقالية، ولكنها تميل إلى أن تكون أضعف، وموصليتها أقل من المعادن الانتقالية.
- أشباه الفلزات: تضم هذه المجموعة البورون (B)، والسيليكون (Si)، والجرمانيوم (Ge) ، والزرنيخ (As)، والأنتيمون (Sb)، والتيلوريوم (Te)، والبولونيوم (Po)، وهي تتصرف كأشباه موصلات أحياناً بدلاً من كونها موصلات، وتسمى المعادن أيضا “أشباه المعادن”.
- اللافلزات: يستخدم مصطلح “اللافلزات” لللتعبير عن كل من الهيدروجين (H)، والكربون (C)، والنيتروجين (N)، والفوسفور (P)، والأكسجين (O)، والكبريت (S)، والسيلينيوم (Se).
- الهالوجينات: عناصر الهالوجين هي مجموعة فرعية من اللافلزات، وهي تتألف من المجموعة 17 من الجدول الدوري، ابتداءاً من الفلور (F) إلى استاتين (At)، وهي شديدة التفاعل كيميائياً، وموجودة في البيئة كمركبات بدلاً من عناصر نقية.
- الغازات النبيلة: تتكون الغازات الخاملة أو النبيلة من المجموعة 18، وهي مستقرة كيميائياً عامةً، وتظهر خصائص متشابهة لكونها عديمة اللون وعديمة الرائحة.
تضم العناصر الكيميائية ما يلي:[٤]
- الهيدروجين (H).
- الهيليوم (He).
- الليثيوم (Li).
- البريليوم (Be).
- البورون (B).
- الكربون (C).
- النيتروجين (N).
- الأكسجين (O).
- الفلور(F).
- النيون (Ne).
- الصوديوم (Na).
- المغنيسيوم (Mg).
- الألمنيوم (Al).
- السيليكون (Si).
- الفوسفور (P).
- الكبريت (S).
- الكلور (Cl).
- أرغون(Ar).
- البوتاسيوم (K ).
- الكالسيوم (Ca).
- السكانديوم (Sc).
- التيتانيوم (Ti).
- فاناديوم (V).
- الكروم(Cr).
- الماغنيسيوم (Mn).
- الحديد (Fe).
- الكوبالت (Co).
- النيكل (Ni).
- النحاس (Cu).
- الزنك (Zn).
- الجاليوم (Ga).
- جيرمانيوم (Ge).
- زرنيخ (As).
- سيلينيوم (Se).
- البروم (Br).
- الكريبتون (Kr).
- الروبيديوم (Rb).
- سترونشيوم (Sr).
- إتريوم (Y).
- زركونيوم (Zr).
- النيوبيوم (Nb).
- موليبدنوم (Mo).
- تكنيشيوم (Tc).
- الروثينيوم (Ru).
- الروديوم (Rh).
- بالاديوم (Pd).
- الفضة (Ag)
- كادميوم ( Cd).
- الإنديوم (In).
- القصدير (Sn.
- إثمد (Sb).
- تيلوريوم (Te).
- يود (I).
- زينون (Xe).
- سيزيوم (Cs ).
- لانثانوم (Ba).
- سيريوم (La).
- براسوديميوم (Ce).
- براسوديميوم (Pr).
- نيوديميوم (Nd).
- بروميثيوم (Pm).
- ساماريوم (Sm ).
- يوروبيوم (Eu).
- جادولينيوم (Gd).
- تيربيوم (Tb).
- ديسبروسيوم (Dy).
- هولميوم (Ho).
- إربيوم (Er).
- توليوم (Tm).
- إتيربيوم (Yb).
- لوتيشيوم (Lu).
- هافنيوم (Hf).
- تانتالوم (Ta).
- تنجستن (W).
- رينيوم (Re).
- أوزميوم (Os).
- إريديوم (Ir).
- بلاتين (Pt).
- ذهب (Au).
- زئبق (Hg).
- ثاليوم (Ti).
- رصاص (Pb).
- بزموت (Bi).
- بولونيوم (Po).
- أستاتين (At).
- راديون (Rn).
- فرانسيوم (Fr).
- راديوم (Ra).
- أكتينيوم (Ac).
- ثوريوم (Th).
- بروتكتينيوم (Pa).
- يورانيوم (U).
- نبتونيوم (Np).
- بلوتونيوم (Pu).
- أمريسيوم (Am).
- كوريوم (Cm).
- بركيليوم (Bk).
- كاليفورنيوم (Cf).
- أينشتاينيوم (Es).
- فرميوم (Fm).
- مندليفيوم (Md).
- نوبليوم (No).
- لورنسيوم (Lr).
- رذرفورديوم (Rf).
- دوبنيوم (Db).
- سيبورغيوم (Sg).
- بوريوم (Bh).
- هاسيوم (Hs).
- مايتنريوم (Mt).
- رونتيجينيوم (Rg).
- كوبرنيسيوم (Cn).
- أنون تريوم (Uut).
- فليروفيوم (Uuq).
- أنون بنتيوم (Uup).
- ليفرموريوم (Uuh).
- أنون سبتيوم (Uus).
- أنون أوكتيوم (Uuo).
- ↑ “List of chemical elements”, www.britannica.com, Retrieved 5-7-2018. Edited.
- ↑ Anne Marie Helmenstine (17-4-2018), “What Is an Element in Chemistry? Definition and Examples”، www.thoughtco.com, Retrieved 5-7-2018. Edited.
- ↑ “How Are Elements Grouped?”, www.livescience.com,5-4-2013، Retrieved 5-7-2018. Edited.
- ↑ Anne Marie Helmenstine (1-4-2018), “Element List – Names, Atomic Numbers, Element Symbols”، www.thoughtco.com, Retrieved 5-7-2018. Edited.