محتويات
'); }
تعريف الأحماض والقواعد
يُعدّ عالم الكيمياء روبرت بويل (بالإنجليزية: Robert Boyle) أول من قام بتصنيف المواد إلى أحماض (بالإنجليزية: Acids) وقواعد (بالإنجليزية: Bases) في القرن السابع عشر، وأطلق على القواعد اسم القلويات، وقد صنّفها اعتماداً على عدد من الخصائص، إذ عرّف الأحماض على أنّها مواد طعهما حامض، وتسبب تآكل المعادن، وتحول ورقة عباد الشمس إلى الأحمر، وتقل حامضيتها عند خلطها مع القواعد، وعرّف القواعد بأنّها مواد ذات ملمس زلق، وتحول ورقة عباد الشمس إلى الأزرق، وتقل قاعديتها عند خلطها مع الأحماض، وقد حاول العلماء فيما بعد -من ضمنهم بويل- توضيح سلوك الأحماض والقواعد وكيفية عملها، لكن لم يتمّ اقتراح أي تعريف منطقي للأحماض والقواعد إلّا في القرن التاسع عشر.[١]
تعريف أرهنيوس
قدّم العالم السويدي سفانت أرهنيوس (بالإنجليزية: Svante Arrhenius) في أواخر القرن التاسع عشر مقترحاً تضمن أنّ الماء قادر على إذابة بعض المركبات وتفكيكها إلى أيّونات منفردة، وبذلك عرّف الأحماض على أنّها مركبات تحتوي على عنصر الهيدروجين وتتفكك في الماء لإطلاق أيون الهيدروجين إلى المحلول، فمثلاً عند إذابة حمض الهيدروكلوريك (HCl) في الماء يَنتِج أيون الهيدروجين (+H) وأيون الكلوريد (–Cl) على النحو الآتي:[١]
'); }
HCl in H2O → H+ (aq) + Cl–(aq)
بينما عرّف القواعد على أنّها مركبات تذوب في الماء وتتفكك لتُطلق أيونات الهيدروكسيد (–OH) إلى المحلول، فعلى سبيل المثال عند إذابة القاعدة هيدروكسيد الصوديوم في الماء ينتج أيون الهيدروكسيد (–OH)، وأيون الصوديوم (+Na) على النحو الآتي: [١]
(aq)–NaOH in H2O → Na+ (aq) + OH
وقدّم تعريف أرهنيوس توضيحاً لأساسيات كيمياء الأحماض والقواعد، ووضحت نظريته العديد من الأمور، منها :[١]
- تمتلك جميع الأحماض والقواعد خصائص متشابهة فيما بينها؛ لأنّ جميع الأحماض تُطلق أيون الهيدروجين إلى المحاليل، وتُطلق جميع القواعد أيون الهيدروكسيد إلى المحاليل.
- تؤثر كل من الأحماض والقواعد على بعضها البعض عندما تتفاعل معاً، بحيث تُضعف القاعدة من تأثير الحمض والعكس صحيح، وتسمى هذه التفاعلات تفاعلات التعادل (بالإنجليزية: Neutralization)، وقد استنتج هذه الفكرة من خلال شرحه لملاحظات بويل.
وعلى الرغم من ذلك لم تستطِع نظريته تفسير سلوك بعض المواد، فمثلاً يتصرف مركب بيكربونات الصوديوم (NaHCO3) بطريقة تشبه القاعدة في حين أنّه لا يحتوي على أيون الهيدروكسيد.[١]
تعريف برونستد- لوري
نشر العالم الدنماركي يوهانس برونستد (بالدنماركية: Johannes Brønsted)، والعالم الإنجليزي توماس لوري (بالإنجليزية: Thomas Lowry) عام 1932م أبحاثاً مُستلقة لكنها متشابهة تضمّنت تنقيحاً لنظرية أرهنيوس للأحماض والقواعد، إلّا أنّ تعريف برونستد- لوري كان أشمل، والذي ينص على: “الحمض هو أيّ مادة يُمكنها التبرع بأيون الهيدروجين، ويُسمى غالباً متبرع البروتون؛ لأنَّ أيون الهيدروجين يشبه في تصرفه هذا تصرف البروتون، إذ إنّه يفقد إلكتروناً”، وهذا يتوافق مع تعريف أرهنيوس إلى حد ما، بينما يختلف مفهوم القاعدة بالنسبة لهما تماماً عن مفهوم أرهنيوس، إذ عرّف القاعدة على أنّها أيّ مادة قادرة على استقبال أيون الهيدروجين، بناءً على ذلك يُعدّ هيدروكسيد الصوديوم مادة قاعدية؛ لأنّه يستقبل أيون الهيدروجين من الحمض لإنتاج الماء، كما استطاع مفهوم برونستد-لوري توضيح سلوك المواد التي تتصرف كالقواعد ولكنها لا تحوي أيون الهيدروكسيد، ومثال على ذلك مركب بيكربونات الصوديوم، والذي يتفاعل حسب المعادلة الآتية:[١]
-
-
-
-
- HCl + NaHCO3→ H2CO3 + NaCl
-
-
-
لقد استقبلت القاعدة (بيكربونات الصوديوم) أيون الهيدروجين من حمض الهيدروكلوريك، ونتج عن هذا التفاعل ملح كلوريد الصوديوم (NaCl)، وحمض الكربونيك (H2CO3) الذي يتفكك سريعاً ليُنتِج الماء، وغاز ثاني أكسيد الكربون، ويستدل على وجود الغاز بظهور فقاعات في المحلول.[١]
وعلى الرغم من هذه التفسيرات، إلّا أنّ مفهوم برونستد-لوري عجز عن تفسير سلوك بعض المركبات التي لا تحتوي على عنصر الهيدروجين إلّا أنّها تمتلك خواص الأحماض، ومثال على ذلك ثلاثي فلوريد البورون (BF3)، وكلوريد الألومنيوم (AlCl3).[٢]
تعريف لويس
لم يَستخدِم العالم جيلبرت لويس (بالإنجليزية: Gilbert Lewis) البروتون لتعريف الأحماض والقواعد، وإنّما استخدَم فقط أزواج الإلكترونات، وعليه فإنّ الحمض بحسب تعريف لويس هو مركب يستقبل زوج الإلكترونات، بينما القاعدة هي مركب قادر على منح زوج الإلكترونات، وعلى الرغم من أنّ هذا التعريف الأقل تقييداً للأحماض والقواعد[٣] إلّا أنّ النظرية فشلت في تفسير تفاعلات الأحماض والقواعد التي لا تتضمن تكوين رابطة تساهمية تناسقية.[٢]
خصائص الأحماض والقواعد
وصف روبرت بويل الأحماض والقواعد بعدة خصائص تُستخدم للتمييز بين الحموض والقواعد الكيمائية دون الحاجة إلى إجراء اختبارات مُعقدة لذلك، منها:[٣]
- مذاق الأحماض حامض، حيث إنّ كلمة (Acid) باللغة اللاتينية تعني حادة أي أنّها حامضة، بينما مذاق القواعد مُرّ، لكن لا يجب تذوقهما.
- الأحماض تُغيّر لون ورقة عباد الشمس الزرقاء إلى اللون الأحمر، بينما لا تُغيّر القواعد لون ورقة عباد الشمس؛ لكنّها تُغيّر ورقة عباد الشمس القاعدية الحمراء إلى اللون الأزرق.
- عند تفاعل الأحماض مع معدن نشط مثل: المعادن القلوية، والمعادن القلوية الأرضية، والزنك، والألومنيوم) تُحرّر غاز الهيدروجين.
- القواعد ملمسها زلق كالصابون، لكن لا يجب لمسها.
- لدى الأحماض والقواعد خصائص مشتركة؛ إذ تتفاعل مع بعضها البعض لإنتاج الماء والأملاح.
- محاليل الأحماض والقواعد قادرة على توصيل التيار الكهربائي.
- مُعظم الأحماض والقواعد القوية تُسبب حروقاً شديدة عند ملامستها للجلد.[٤]
- مُعظم الأحماض والقواعد القوية مواد تسبب التآكل في الطبيعة، إذ تميل إلى تآكل المواد وتكوين الصدأ.[٤]
الأحماض والقواعد القوية والضعيفة
تُعرّف الأحماض القوية على أنّها مركبات جزيئية تتأيّن بشكل كامل في محاليلها المائية، بحيث تتفكك إلى أيون الهيدروجين، وأيون سالب الشحنة (Anion)، وتجدر الإشارة إلى أنّ عدد الأحماض القوية الشائعة محدود جداً، أمّا الأحماض الضعيفة لا تتأيّن بالكامل في محاليلها، ومثال عليها حمض الأسيتيك (CH3COOH) فهو لا يتفكك في الماء إلّا بنسبة مئوية قليلة، وتعتمد هذه النسبة على تركيزه ووجوده في المحلول، وغالباً ما يوجد على شكل جزئيات غير منفصلة، وفيما يأتي توضيح لأنواع الأحماض:[٥]
- الأحماض القوية: مثل: حمض الهيدروكلوريك (HCl)، وحمض الهيدرويوديك (HI)، وحمض الهيدروبروميك (HBr)، وحمض النيتريك (HNO3)، وحمض الكبريتيك (H2SO4)، وحمض البيركلوريك (HClO4).
- الأحماض الضعيفة: أيّ حمض آخر، مثل: حمض الهيدروسيانيك (HCN)، وحمض كبريتيد الهيدروجين (H2S)، وحمض الميثانويك (HCOOH)، وحمض الهيدروفلوريك (HF).
ينطبق الأمر على القواعد كما ينطبق على الأحماض، فالقاعدة القوية تتأيّن بشكل كامل في المحاليل المائية، فتنفصل إلى أيونات بشكل تام، وتُصنّف القواعد القوية حسب مدى تأيّنها، وعلى غرار الأحماض القوية فإنّ هناك عدد محدود منها، أمّا القواعد الضعيفة فهي مركبات جزيئية لا تتأيّن بشكل كامل في المحاليل المائية، وفيما يأتي توضيح لأنوعيهما:[٥]
- القواعد القوية: تُمثّل هيدروكسيدات عناصر المجموعة الأولى والمجموعة الثانية من الجدول الدوري، ومن الأمثلة عليها: هيدروكسيد الليثيوم (LiOH)، وهيدروكسيد الصوديوم (NaOH)، وهيدروكسيد البوتاسيوم (KOH)، وهيدروكسيد السيزيوم (CsOH)، وهيدروكسيد الروبيديوم (RbOH).
- القواعد الضعيفة: أيّ قاعدة أخرى، مثل: الأمونيا (NH3)، وميثيل أمين (CH3NH2)، والبَيريدِين (C5H5N).
الرقم الهيدروجيني
واجه الكيميائيون مشاكل في حساب تراكيز أيونات الهيدرونيوم (+H3O) عند عملهم بالأحماض، حيث إنّ جميع الأرقام في حساباتهم كانت تحتوي على أُسس سالبة، ومن هنا جاءت فكرة الرقم الهيدروجيني (pH) لحل هذه المشكلة، فقد اقترح عالم الكيمياء الدنماركي سورين سورينسن (بالإنجليزية: Soren Sorensen) عام 1909م استخدام اللوغاريتم السالب لتركيز أيون الهيدرونيوم لقياس حامضية المواد، وأطلق على هذا المقياس اسم (pH)، ويَرمز الحرف (p) إلى قوة العدد (الأُس)، بينما يَرمز الحرف (H) إلى عنصر الهيدروجين.[٦]
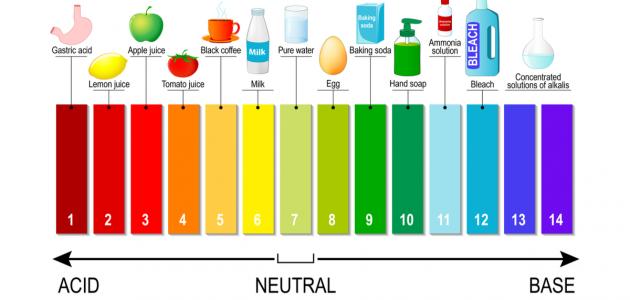
وتُجدر الإشارة إلى أنّ الرقم الهيدروجيني هو مجرد مؤشر فقط للتعبير عن مدى حمضية أو قاعدية المحلول، ويتدرج المقياس من أدنى قيمة مُمكنة له وهي 0 إلى أعلى قيمة مُمكنة له وهي 14، وتشير القيم التي تقع بين (0-6) إلى أنّ المادة حمضية، بينما تشير القيم التي تقع بين (8-14) إلى أنّ المادة قاعدية، ولكن تشير القيمة 7 إلى أنّ المادة متعادلة.[٦]
محاليل الأحماض والقواعد
محاليل الأحماض
تُكوّن الأحماض محاليلها عن طريق إنتاجها لأيون الهيدروجين والأيون السالب الآخر، ويُمكن توضيح تكوين المحاليل الحمضية من خلال المعادلة العامة الآتية، حيث يُمثّل (A) الأيون السالب:[٧]
-
-
-
-
- –HA → H+ + A
-
-
-
ومن الأمثلة عليها:[٧]
- محلول حمض الهيدروكلوريك: –HCl → H+ + Cl
- محلول حمض النيتريك: –HNO3 → H+ + NO3
- محلول حمض الأسيتيك: –CH3COOH → H+ + CH3COO
محاليل القواعد
تُعدّ القواعد مركبات أيونيّة تُنتِج أيون الهيدروكسيد (–OH) السالب في محاليلها من كل من: الهيدروكسيد (–OH)، والأكسيد (–O2)، والكربونات (CO3-2)، والبيكربونات (–HCO3)، ويُمكن توضيح تكوين المحاليل الحمضية من خلال المعادلة العامة الآتية، حيث يُمثّل (M) الأيون الموجب:[٧]
-
-
-
-
- –MOH → M+ + OH
-
-
-
ومثال على ذلك محلول هيدروكسيد الصوديوم: –NaOH → Na+ + OH
ويُعدّ تكوين المحاليل القاعدية من الأكاسيد، والكربونات، والبيكربونات مُعقد أكثر، لكنّها تتفاعل مع الماء لتُنتج أيون الهيدروكسيد، ومن الأمثلة عليها:[٧]
- محلول أكسيد الصوديوم: –Na2O + H2O → Na+ + OH
- محلول كربونات الصوديوم: –Na2CO3 + H2O → H2CO3 + Na+ + OH
- محلول بيكربونات الصوديوم: –NaHCO3 + H2O → H2CO3 + Na+ + OH
تفاعلات الأحماض والقواعد
تُعرَف التفاعلات الكيميائية بين الأحماض والقواعد بنسب متساوية بتفاعلات التعادل (بالإنجليزية: Neutralisation Reactions)، وهذا يعني أنّ كمية أيونات الهيدروجين وأيونات الهيدروكسيد الداخلة في التفاعل تكون متساوية، ما يُنتِج محلولاً متعادلاً يتكون من الماء، والملح، مثل أملاح: كلوريد الصوديوم (NaCl)، وكبريتات المغنيسيوم (MgSO4)، وأسيتات البوتاسيوم (KCH3COO)، وحسب نوع القاعدة الداخلة في التفاعل قد ينتج ثاني أكسيد الكربون، وفي حال تفاعلت المواد الناتجة من التفاعل (نواتج التفاعل) مع الماء ينتج عنها محاليل ذات تأثير قاعدي أو حمضي.[٧]
توجد أربعة أنواع رئيسية لتفاعلات الأحماض والقواعد تختلف بحسب نوع القاعدة الداخلة في التفاعل، وهي:[٧]
- تفاعل بين الحمض وهيدروكسيدات المعادن: يُنتِج هذا التفاعل الماء والأملاح، ومثال على ذلك يتفاعل حمض الهيدروكلوريك (HCl) مع القاعدة هيدروكسيد الصوديوم (NaOH) ليَنتج ملح كلوريد الصوديوم (NaCl) والماء، حسب المعادلة الآتية:
-
-
-
-
- HCl + NaOH → NaCl + H2O
-
-
-
- تفاعل الحمض وأكاسيد المعادن: يُنتِج هذا التفاعل الملح والماء، ومثال على ذلك يتفاعل حمض الهيدروكلوريك (HCl) مع أكسيد الصوديوم (Na2O) ليَنتج ملح كلوريد الصوديوم (NaCl) والماء، حسب المعادلة الآتية:
-
-
-
-
- HCl + Na2O → NaCl + H2O
-
-
-
- تفاعل الحمض وكربونات المعادن: يُنتِج هذا التفاعل الملح والماء، بإلاضافة إلى غاز ثاني أكسيد الكربون، ومثال على ذلك يتفاعل حمض الهيدروكلوريك (HCl) مع كربونات الصوديوم (Na2CO3) ليَنتج ملح كلوريد الصوديوم (NaCl)، والماء، وغاز ثاني أكسيد الكربون، حسب المعادلة الآتية:
-
-
-
-
- HCl + Na2CO3 → NaCl + CO2 + H2O
-
-
-
- تفاعل الحمض وبيكربونات المعادن: يُنتِج هذا التفاعل الملح، والماء، بإلاضافة إلى غاز ثاني أكسيد الكربون، ومثال على ذلك يتفاعل حمض الهيدروكلوريك (HCl) مع بيكربونات الصوديوم (NaHCO3) ليَنتج ملح كلوريد الصوديوم (NaCl)، والماء، وغاز ثاني أكسيد الكربون، حسب المعادلة الآتية:
-
-
-
-
- HCl + NaHCO3 → NaCl + CO2 + H2O
-
-
-
كواشف الأحماض والقواعد
تُعرّف كواشف على أنّها أحماض أو قواعد ضعيفة يتغيّر لونها تبعاً للرقم الهيدروجيني (pH)، كما تُعرَف أيضاً بمؤشر الرقم الهيدروجيني، وفيما يأتي جدول يبيّن بعض أنواع الكواشف الكيميائية، وتغيّر ألوانها تبعاً للمادة سواءً أكانت حمضية أم قاعدية: [٨]
| اسم الكاشف | لونها في الحمض | لونها في القاعدة | ثابت الحموضة (pK)* | مدى الرقم الهيدروجيني (pH) |
|---|---|---|---|---|
| أزرق الثايمول- تحول أول | أحمر | أصفر | 1.5 | 1.2-2.8 |
| برتقالي الميثيل | أحمر | أصفر | 3.7 | 3.2-4.4 |
| أخضر البروموكريسول | أصفر | أزرق | 4.7 | 3.8-5.4 |
| أحمر الميثيل | أصفر | أحمر | 5.1 | 4.8-6.0 |
| أزرق البروموثايمول | أصفر | أزرق | 7.0 | 6.0-7.6 |
| أحمر الفينول | أصفر | أحمر | 7.9 | 6.8-8.4 |
| أزرق الثايمول- تحول ثاني | أصفر | أزرق | 8.9 | 8.0-9.6 |
| فينول فثالين | عديم اللون | أرجواني | 9.4 | 8.2-10.0 |
بعض استخدامات الأحماض والقواعد
تُستخدم العديد من الأحماض والقواعد على نطاق واسع في عدة مجالات، وفيما يأتي استخدامات بعض أنواع الأحماض:[٢]
- يُستخدَم حمض الأسيتيك والذي يُعرف بالخل كمحلول مُخفف في العديد من الاستخدامات المنزلية، وبشكل أساسي في حفظ الأغذية.
- يُعدّ حمض الستريك جزءاً رئيسياً من عصير الليمون والبرتقال، ويُمكن استخدامه في حفظ الطعام.
- يُستخدَم حمض الكبريتيك بشكل كبير في صناعة البطاريات.
- يُستخدَم كل من حمض الكبريتيك وحمض النيتريك في عمليات تصنيع المتفجرات، والأصباغ، والدهانات، والأسمدة.
- يُعدّ حمض الفوسفوريك عنصراً رئيسياً في المشروبات الغازية.
- يُستخدَم حمض الهيدروكلوريك في صناعات الصُلب لتنظيف الصفائح المعدنية قبل البدء بعملية مُعالجتها.[٩]
تُستخدَم العديد من أنواع القواعد في العديد من المجالات، منها:
- يُستخدَم هيدروكسيد المغنيسيوم، والذي يُعرف باسم حليب المغنيسيا كمُضاد للحموضة، إذ يقلل من الحموضة الزائدة في المعدة، كما يُستخدَم كمُليّن للأمعاء.[٢]
- يُعدّ هيدروكسيد الأمونيوم أحد الكواشف الهامة التي تُستخدَم في المختبرات.[٢]
- يُستخدَم هيدروكسيد الصوديوم في صناعة الحرير الصناعي، وصناعة الصابون والورق[٢] لإزالة اللغنين من لب الورق، كما يُستخدَم من قبل منتجي الأغذية كعامل كيميائي مساعد لتقشير الفواكه.[٩]
- يُستخدَم هيدروكسيد الكالسيوم الذي يُعرف باسم الجير المطفأ في تصنيع مسحوق التبييض، كما يُستخدَم في معادلة حموضة التربة الزائدة، بالإضافة إلى ذلك يُستخدَم في تصنيع الخلطات الجافة للدهان والزخرفة،[٢] كما يُستخدَم كملاط بين الطوب في عمليات البناء.[٩]
- تُستخدَم بيكربونات الصوديوم التي تُعرف بصودا الخبز كأحد المكونات الأساسية في وصفات الخَبز.[٩]
ــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
- ثابت الحموضة أو ثابت تفكك الحمض: مقياس كمي لقوة الحمض في المحلول).[١٠]
المراجع
- ^ أ ب ت ث ج ح خ ANTHONY CARP, “Acids and Bases”، www.visionlearning.com, Retrieved 2-1-2020. Edited.
- ^ أ ب ت ث ج ح خ “Acids And Bases”، byjus.com،Retrieved 2-1-2020. Edited
- ^ أ ب Anne Marie Helmenstine (5-5-2019)، “?What Are Acids and Bases”، www.thoughtco.com، Retrieved 2-1-2020. Edited
- ^ أ ب “Similarity Between Acids And Bases”, www.toppr.com, Retrieved 2-1-2020. Edited.
- ^ أ ب “Overview of Acids and Bases”, chem.libretexts.org,29-9-2019، Retrieved 2-1-2020. Edited.
- ^ أ ب Amy Meyers, “The pH Scale”، study.com, Retrieved 7-1-2020. Edited.
- ^ أ ب ت ث ج ح “Acid-Base Reactions”, www.goodscience.com.au, Retrieved 3-1-2020. Edited.
- ↑ “Acid – Base Indicators”, www.chemistry.bd.psu.edu, Retrieved 3-1-2020. Edited.
- ^ أ ب ت ث Doug Johnson (26-4-2018), “Uses of Acids & Bases”، www.sciencing.com, Retrieved 3-1-2020. Edited.
- ↑ Anne Marie Helmenstine (25-5-2019), “Acid Dissociation Constant Definition: Ka”، thoughtco.com, Retrieved 2-2-2020. Edited.