محتويات
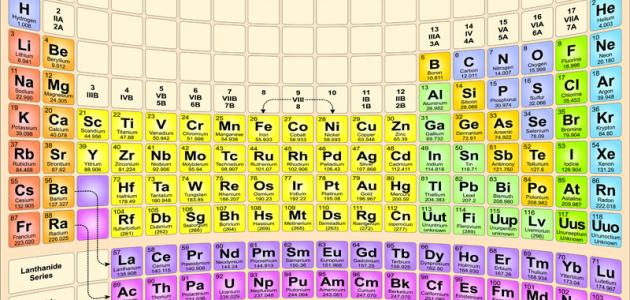
تتحلى اللافلزات بالكثير من الخصائص التي تختلف تماماً عن خصائص الفلزات ومنها:[١]
- لها درجة غليان ودرجة انصهار منخفضة.
- ضعيفة التوصيل الحراري.
- ضعيفة التوصيل الكهربائي.
- تمتلك طاقة تأيّن عالية جداً تساعدها في جذب الإلكترونات إليها.
- تتمتع ببريق معدني قليل جداً يكاد يكون معدوماً.
- تعتبر اللافلزات الصلبة هشّة جداً لايمكن طرقها وتشكيلها.
- تتحد مع الأكسجين مكوّنةً أكاسيد حمضيّة.
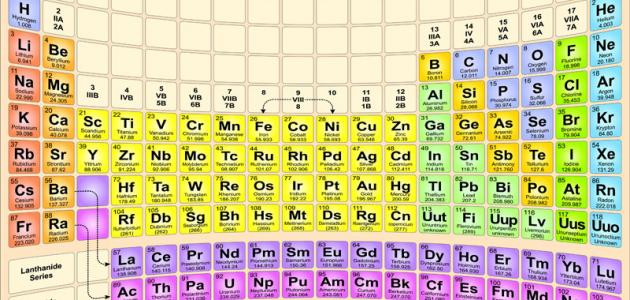
هي عناصر كيميائيّة غير معدنيّة، لاتتواجد بكثرة في الطبيعة مثل الفلزات، لكنها تعد ضروريّة جداً لنمو الكائنات الحيّة، معظم اللافلزات ذراتها صغيرة الحجم، وتحتوي على عدد كبير من الإلكترونات التي تدور حول نواتها.[٢] تتواجد اللافلزات في الجدول الدوري في الجهة اليمنى من الأعلى على شكل مثلث، وتشتمل على الغازات النبيلة، الهالوجينات،وثمانية عناصر تسمى باليتيمة تشتمل على عنصري الكربون والهيدروجين، وتعد ضرورية جداً للحياة، حيث تشكل اللافلزات مثل الهيدروجين والأكسجين مايقارب 99% من كتلة الكون المحيط بنا.[٣]
من أهم اللافلزات العناصر الكيميائية التالية:[٣]
- عنصر البورون ذو العدد الذري 5.
- عنصر النيتروجين ذو العدد الذري 7.
- عنصر الأكسجين ذو العدد الذري 8.
- عنصر الفسفور ذو العدد الذري 15.
- عنصر الكبريت ذو العدد الذري 16.
- عنصر السيلينيوم ذو العدد الذري 34.
سميت الغازات النبيلة بذلك بسبب عدم ميلها للتفاعل والارتباط بالعناصر الأخرى، حيث تتواجد في الطبيعة على شكل ذرات فردية وليس جزيئات وتسمى أيضاً بالعناصر الخاملة وهي:[٣]
- الهيليوم (He).
- النيون (Ne).
- الآرجون (Ar).
- الكريبتون (Kr).
- الزينون (Xe).
- الرادون (Rn).
تحتل الهالوجينات المجموعة السابعة في الجدول الدوري للعناصر وهي أكثر المجموعات تنوّعاً في حالة عناصرها، فمنها ماهو صلب ومنها ماهو غازي، كما تعد الأنشط في التفاعل مع العناصر الأخرى، إذ تمتلك أعلى كهروسلبيّة وميلا لجذب إلكترونات التكافؤ والارتباط بها، وهي:[٣]
- الفلور (F).
- الكلور (Cl).
- البرومين (Br).
- اليود (I).
- الاستاتين (At).
- ↑ Anne Marie Helmenstine, Ph.D. (20-4-2018), “The Definition and Properties of Nonmetals”، www.thoughtco.com, Retrieved 4-9-2018. Edited.
- ↑ “Nonmetal”, www.britannica.com, Retrieved 4-9-2018. Edited.
- ^ أ ب ت ث “NONMETALS”, www.encyclopedia.com, Retrieved 4-9-2018. Edited.